Актуальные проблемы анестезиологии, реаниматологии и интенсивной терапии.
Материалы научной конференции. Под редакцией В.И. Cтрашнова.
Санкт-Петербург, 2001
Содержание
- ЭФФЕКТИВНОСТЬ И БЕЗОПАСНОСТЬ ПРИМЕНЕНИЯ
ЛИКВОРОСОРБЦИИ У НЕЙРОХИРУРГИЧЕСКИХ БОЛЬНЫХ В
РАННЕМ ПОСЛЕОПЕРАЦИОННОМ ПЕРИОДЕ
Р. В. Назаров
Отдел анестезиологии и реанимации Российского
научно-исследовательского нейрохирургического
института имени проф. А. Л. Поленова
- ПЕРВЫЙ ОПЫТ ПРИМЕНЕНИЯ КОЛЛОИДНОГО
КРОВЕЗАМЕНИТЕЛЯ АНТИГИПОКСИЧЕСКОГО ДЕЙСТВИЯ
ПОЛИОКСИФУМАРИНА В КАЧЕСТВЕ ОСНОВЫ
КАРДИОПЛЕГИЧЕСКОГО РАСТВОРА ПРИ ОПЕРАЦИЯХ В
УСЛОВИЯХ ИСКУССТВЕННОГО КРОВООБРАЩЕНИЯ
К.Ю. Сенчик, В.В. Гриценко, В.Н. Чуфаров, Д.Н.
Дойников, О.Ю. Мочалов, Г. Г. Юрлова, В.М. Мирошкина,
Т. И. Щербак
Кафедра анестезиологии, реаниматологии и
интенсивной терапии СПбГМУ имени академика И.П.
Павлова
- СОЧЕТАННАЯ КОМБИНИРОВАННАЯ СПИНАЛЬНАЯ И
ЭПИДУРАЛЬНАЯ АНЕСТЕЗИЯ КАК СРЕДСТВО АНАЛИЗА И
ПРЕДУПРЕЖДЕНИЯ НЕЙРОДИСТРОФИЧЕСКОГО КОМПОНЕНТА
ПОСЛЕОПЕРАЦИОННЫХ ОСЛОЖНЕНИЙ
В. И. Страшное, О. И. Забродин, А.Д. Мамедов
Кафедра анестезиологии, реаниматологии и
интенсивной терапии СПбГМУ имени академика И.П.
Павлова
ЭФФЕКТИВНОСТЬ И БЕЗОПАСНОСТЬ ПРИМЕНЕНИЯ
ЛИКВОРОСОРБЦИИ У НЕЙРОХИРУРГИЧЕСКИХ БОЛЬНЫХ В
РАННЕМ ПОСЛЕОПЕРАЦИОННОМ ПЕРИОДЕ
Р. В. Назаров
Отдел анестезиологии и реанимации Российского
научно-исследовательского нейрохирургического
института имени проф. А. Л. Поленова
Доказано, что накопление в спинномозговой
жидкости патологических субстратов (излившейся
крови, поврежденной мозговой ткани и продуктов
ее распада) ведет к утяжелению состояния
нейрохирургических больных, ухудшению течения
заболевания, углублению гемоциркуляторных
нарушений в центральной нервной системе.
Естественная элиминация патологических веществ
из ликвора происходит, как правило, в течение
длительного времени (2-4 недели).
В связи с этим в комплексе реанимационных
мероприятий все большее применение находят
методы активной санации субарах-ноидального
пространства. Эти методы позволяют удалить
токсичные продукты распада мозгового детрита
(сывороточные белки, клетки крови и вещества,
выделяющиеся в процессе их деструкции),
восстановить проходимость ликворных путей и
стабилизировать перфузионное давление мозга-
Механическая санация не может быть эффективно
осуществлена при использовании рутинных
методов. К тому же используемые при активной
санации растворы не соответствуют ликвору по
электролитному, кислотно-основному,
гормональному и иммунному составу и оказывают
негативное влияние на нервную ткань. Это
определяет интерес к использованию
ликворосорбции (ЛС) в раннем послеоперационном
периоде у нейрохирургических больных. Однако,
возможные осложнения при активном вмешательстве
в ликвородинамику у данной категории больных
сужают показания к использованию ЛС.
Среди наиболее грозных осложнений, описанных в
литературе, отмечаются: повторный разрыв
внутричерепных аневризм, дислокация структур
головного мозга, гнойно-воспалительные
осложнения, повреждение головного и спинного
мозга при пункции лик-воросодержащих
пространств.
Система для рециркуляторной ЛС состоит из двух
колонок с сорбентом СНК-2К и соединительной
магистрали, по которой посредством роликового
насоса осуществляется движение спинномозговой
жидкости. В каждой колонке помещается 10 см3
сорбента, а общий объем заполнения системы не
превышает 70 мл физиологического раствора.
Процедура была выполнена 20 больным
нейрохирургического профиля, из них 2 больным с
тяжелой черепно-мозговой травмой, 3 больным с
острыми субарахноидальными кровоизлияниями
аневризматической этиологии, 15 больным с
опухолями головного мозга различной
гистоструктуры и локализации. ЛС проводилась на
3-7-е сутки после оперативного вмешательства на
аппарате АКСТЗ-17 со скоростью 1,5 мл/мин в течение
90 минут. Всем больным во время процедуры
осуществлялся мониторинг АД и ЧСС. Выполнялись
рутинные биохимические и микроскопические
анализы ликвора и крови пациентов до и после
сорбции.
В большинстве случаев (у 17 больных) произошло
отчетливое улучшение лабораторных показателей
спинномозговой жидкости. Кроме того, у 7 больных
(35%) в течение двух суток после процедуры
отмечалась положительная динамика в
неврологическом статусе (регресс общемозговой
и/или очаговой симптоматики). Осложнений во время
проведения ликворосорбции не отмечено.
Полученные результаты показали, что ЛС у
нейрохирургических больных является
малоинвазивной, безопасной операцией.
Применение ее в раннем послеоперационном
периоде обеспечивает максимально быстрое
уменьшение эндогенной интоксикации и
восстановление нарушенных функций ЦНС.
ПЕРВЫЙ ОПЫТ ПРИМЕНЕНИЯ КОЛЛОИДНОГО
КРОВЕЗАМЕНИТЕЛЯ АНТИГИПОКСИЧЕСКОГО ДЕЙСТВИЯ
ПОЛИОКСИФУМАРИНА В КАЧЕСТВЕ ОСНОВЫ
КАРДИОПЛЕГИЧЕСКОГО РАСТВОРА ПРИ ОПЕРАЦИЯХ В
УСЛОВИЯХ ИСКУССТВЕННОГО КРОВООБРАЩЕНИЯ
К.Ю. Сенчик, В.В. Гриценко, В.Н. Чуфаров, Д.Н.
Дойников, О.Ю. Мочалов, Г. Г. Юрлова, В.М. Мирошкина,
Т. И. Щербак
Кафедра анестезиологии, реаниматологии и
интенсивной терапии СПбГМУ имени академика И.П.
Павлова
Цель работы. Оценить защитный,
кардиопротекторный эффект нового
отечественного кровезаменителя
полиоксифумарина в качестве основы для
изготовления кардиоплегического коктейля при
операциях на "сухом" сердце в условиях
тотальной ишемии миокарда (ТИМ) и полного
искусственного кровообращения (ИК) по поводу
врожденных и приобретенных пороков сердца.
Материалы и методы. В клинике госпитальной
хирургии №2 СПбГМУ им. акад. И.П. Павлова (директор
клиники - профессор В-В. Гриценко) выполнены
операции радикальной коррекции пороков сердца в
условиях фармакологической холодовой
кардиопле-гии (ФХКП) и ИК 110 больным. Основную
группу составили 50 больных, у которых защита от
ТИМ осуществлялась с применением
кардиоплегического раствора на основе
полиоксифуиари-на (ПОФ-КП) (30 - врожденные пороки
сердца (ВПС): 18 - дефект межпредсердной
перегородки (ДМПП), 12 - дефект меж-желудочковой
перегородки (ДМЖП) и 20 - приобретенные пороки
сердца (ППС): 12 - комбинированный порок
аортального клапана (КПАК), 8 - комбинированный
порок митрального клапана (КПМК)). Контрольную
группу составили 60 больных у которых
антиишемические мероприятия выполнялись с
применением стандартной ФХКП (модифицированный
р-р St. Tomas) (30 больных с ВПС (15 ДМЖП и 15 ДМПП) и 30
больных с ППС - 15 с КПАК и 15 с КПМК. Возраст больных
с ВПС составлял 7±1,2 года, больных с ППС - 40±б,5 лет.
Больные с ППС обоих групп принадлежали к П-1П
функциональному классу NYHA, а больные с ВПС имели
1-П степень легочной гипертензии.
Кардиопротекторный эффект оценивался по при
нятым в клинике критериям: клинические -
характер восстановления сердечной деятельности,
выраженность нарушения ритма сердца,
потребность в инотропной поддержке, общая
удельная доза симпатомиметиков, сердечный
индекс (СИ), показатели интраопе-рационной
катетеризации камер сердца, выраженность
послеоперационной острой миокардиальной
недостаточности (ОМН); биохимические — уровень
фермента MB КФК в крови; специальные —
температурный профиль миокарда,
ультраструктурный анализ ин-траоперационных
биоптатов миокарда.
Результаты. Время ИК и ТИМ в основной и
контрольной группах не имело достоверных
различий (ВПС: время ИК - 56,4± 7,1 мин;
продолжительность ТИМ - 31,3±4,2 мин; ППС: время ИК —
141,6±8,2 мин, продолжительность ТИМ — 96,5±5,6 мин).
Уровень общей гипотермии для больных с ВПС -
31,6±1,2°С, для больных с ППС - 27,4±1,4°С. Объем ФХКП
рассчитывался по принятой формуле [Сенчик К.Ю- с
соавт., 1995] и составил для больных с ВПС 1,09+0,17 л,
для больных с ППС -2,2±0,1б л и не имел статистически
значимых различий между контрольной и основной
групой. Температура миокарда поддерживалась в
контрольной и основной группах больных на уровне
12,4±1,2°С. Существенные различия между группами
обнаружились в потребности дефибрил-ляции,
которая в основной группе уменьшилась на 35,5% при
ВПС и на 9,8% при ППС. В основной группе сократилось
количество послеоперационных аритмий у больных
ВПС на 2,5%, у больных ППС на 11,2%. Сердечный индекс
вырос в основной группе на 0,28±0,12 л/мУмин у
больных ВПС и на 1,16±0,11 л/м^мин у больных ППС.
Содержание MB КФК в сыворотке крови после
операции у больных ППС основной группы
уменьшилось на 7,3±1,5 ед. Суммарная удельная доза
допамина сократилась в основной группе больных
ВПС на 1,0+0,2 мг/кг, а у больных ППС на 1,4+0,3 мг/кг.
Госпитальная летальность в основной группе
составила 2,3%, в контрольной 6,5%, причем, доля ОМН
как основной причины летального исхода
уменьшилась с 45,5 до 11,2%. Ультраструктурный анализ
интраоперационных кардиобиоптатов показал
улучшение качественных и количественных
характеристик кардиомиоцитов при применении
ПОФ-КП по сравнению с ФХКП.
Выводы. Предложенная и опробированная пропись
ПОФ-КП раствора оказывает выраженный
положительный, по сравнению со стандартной ФХКП,
антиишемический эффект у больных с ВПС и ППС,
оперированных на "сухом" сердце.
СОЧЕТАННАЯ КОМБИНИРОВАННАЯ СПИНАЛЬНАЯ И
ЭПИДУРАЛЬНАЯ АНЕСТЕЗИЯ КАК СРЕДСТВО АНАЛИЗА И
ПРЕДУПРЕЖДЕНИЯ НЕЙРОДИСТРОФИЧЕСКОГО КОМПОНЕНТА
ПОСЛЕОПЕРАЦИОННЫХ ОСЛОЖНЕНИЙ
В. И. Страшное, О. И. Забродин, А.Д. Мамедов
Кафедра анестезиологии, реаниматологии и
интенсивной терапии СПбГМУ имени академика И.П.
Павлова
Оперативные вмешательства на сердце и органах
желудочно-кишечного тракта в клинических
условиях сопровождаются раздражением
рефлексогенных зон и интерорецепторов и
гиперакти-вацией симпатико-адреналовой системы
(САС). В работах школы С.В.Аничкова (З.И.Веденеева,
Н.А.Новикова) электростимуляция рефлексогенной
зоны дуги аорты у крыс и кроликов приводила к
развитию дистрофии миокарда, а в работе И.С.
Заводской механическое раздражение
пилородуоденальной зоны у крыс, морских свинок и
кроликов вызывало развитие изъязвлений
слизистой желудка. Фармакологический анализ
указанных дистрофических изменений обнаружил,
что ведущую роль в их развитии играют
ги-перактивация симпатической нервной системы
(СНС), избыточное высвобождение из симпатических
окончаний медиатора норадрена-лина (НА) и
последующее истощение его содержания [Аничков
С.В. и соавт., 1969; Забродин 0-Н., 1969]. При этом
ганглио-блокаторы и симпатолитики,
препятствующие избыточному возбуждению СНС,
предупреждали развитие указанных
дистрофических повреждений. Следует полагать,
что использование во время операции спинальной
анестезии (СА) и эпидуральной анестезии (ЭА) в
раннем послеоперационном периоде, осуществляя
преганг-лионарную симпатическую блокаду [Hollberg,
Oro, 1964; Bromage, 1967], предупредит гиперактивацию САС и
будет препятствовать развитию в органах,
отмеченных в эксперименте, нейрогенных
дистрофических изменений.
Использование в качестве основного компонента
обезболивания высокой ЭА на уровне ТЬг-ТЬз
[Страшнов В.И., 1968] у больных во время митральной
комиссуротомии предупредило развитие к концу
операции в биопсированном миокарде ушка сердца
дистрофических изменений - истощение содержания
НА и повреждения ультраструктуры клеточных и
внутриклеточных мембран, в частности, мембран
митохондрий кардиомиоцитов [Забродин О.Н. и
соавт., 1981].
Дальнейший анализ механизма
нейродистрофических изменений был связан с
применением в качестве основного компонента
обезболивания сочетанной комбинированной СА у
абдоминальных больных, оперированных по поводу
язвы желудка, двенадцатиперстной кишки,
злокачественных новообразований желудка и
кишечника, желчнокаменной болезни- Использовали
сочетание СА с оксибутиратом натрия, ИВЛ
кислородно-воздушной смесью и однократным
введением миорелаксанта. После предварительной
постановки эпидурального катетера на уровне Thy-g
(с целью послеоперационного обезболивания)
проводили СА. Комбинированная СА состояла в
одноразовом введении больному субарахноидально
на уровне Ь^-Ьз смеси 2% раствора лидокаина (7-8 мл),
фентанила (100 мкг) и клофелина (100 мкг) доз,
достаточных для достижения необходимого уровня
аналгезии (Th^)- Индукция: окси-бутират натрия (4,0-5,0
г) и тиопентал натрия (150-200 мг), миоре-лаксация
ардуаном (4 мг). Интубация трахеи и ИВЛ смесью
воздуха и О; (2 л/мин). Больные контрольной группы
были оперированы в условиях общей анестезии
(нейролептаналгезия + NzO/Oa, ИВЛ).
С учетом того, что активация перекисного
окисления липидов (ПОЛ) является показателем
повреждения клеточных мембран у исследуемых
больных изучали показатели ПОЛ: малоновый
ди-альдегид, диеновые конъюгаты и активность
каталазы (КАТ). Изменения концентрации
малонового диальдегида в крови представлены на
рис. В пробах крови, полученных у контрольных
больных в наиболее травматичный момент операции
и сразу после ее окончания, отмечена заметная
активация перекисных процессов, проявившаяся в
повышении количества малонового диальдегида и
активности КАТ, которые нормализовались только к
утру следующего дня - 2-й, 3-й и 4-й этап
соответственно. У больных основной
группы использование комбинированной
сочетанной СА предупредило активацию ПОЛ и, тем
самым, связанные с ней повреждения клеточных
мембран.
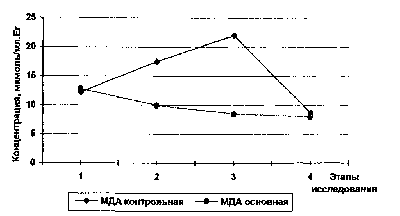
Рис. Изменение концентрации малонового
диальдегида в крови больных основной и
контрольной групп.
Этапы исследования: 1 - перед началом операции; 2
- наиболее трав-матичеый момент операции; 3 - по
окончании операции; 4 - следующее утро после
операции.
Косвенным подтверждением тому явились
результаты оценки активности АЛТ и ACT у тех же
больных. Известно, что повышение активности этих
ферментов связанно с повреждением целостности и
повышением проницаемости клеточных мембран
гепатоци-тов. Подобные нарушения мембран
гепатоцитов (митохондрии, эн-доплазматический
ретикулум) рефлекторного характера были
отмечены при электронно-микроскопическом
исследовании у крыс [Корхов В. В., 1970]. У больных
основной группы, в отличие от больных
контрольной группы, не было отмечено
достоверного повышения активности АЛТ и ACT в
сыворотке крови во время операции, что
свидетельствовало о защитном эффекте СА и ЭА в
отношении мембран гепатоцитов (табл.)-
Таблица
Динамика средних значений биохимических
показателей крови пациентов, оперированных на
органах брюшной полости в условиях сочетанной
комбинированной СА
| Показатель |
Группы |
До операции |
В
реанимации |
Перед
выпиской |
| ACT,
МЕ/л |
контроль |
33,4±11,6 п=31 |
34,2±7,8 п=27 |
36,5±8,2 п=23 |
| основная |
24,6±4 п=14 |
33,2±5 п=13 |
21,5±4,1 п=8 |
| АЛТ,
МЕ/л |
контроль |
35,5±11,4 п=31 |
37,8±11 п=27 |
29,7±9,4 п=23 |
| основная |
16,7±2,6 п=14 |
28,1±4,1 п=13 |
17,1±2,1 п=8 |
Отмеченное увеличение активности ПОЛ, АЛТ и ACT у
больных контрольной группы соответствовало
гиперактивации САС, проявившейся в повышении
экскреции НА и адреналина с мочой во время
операции (см. стр. 32). Использование сочетанной
комбинированной СА во время операции и ЭА в
раннем послеоперационном периоде предупредило
такую гиперактивацию у больных основной группы,
чем можно объяснить защитные эффекты этих видов
регионарной анестезии в отношении развития
дистрофических изменений в органах
Министерство здравоохранения Российской
Федерации. Санкт-Петербургский государственный
медицинский университет имени академика И.II.
Павлова. Актуальные проблемы анестезиологии,
реаниматологии и интенсивной терапии. Материалы
научной конференции. Под редакцией В.И.
Cтрашнова.Санкт-Петербург, 2001, стр. 58 - 62