Сегментарные и проприоспинальные механизмы патогенеза миофасциальных триггерных точек
К.Б. Петров
Кафедра лечебной физкультуры, физиотерапии и курортологии, Новокузнецкий ГИДУВ, Новокузнецк, Россия.
Резюме. При частичном или полном нарушении супраспинального контроля триггерные точки гораздо чаще встречаются в случаях гамма-ригидности и не характерны для альфа-ригидности. Они не зависят от степени поражения спинного мозга и наличия расстройств глубоких или поверхностных видов чувствительности.
У больных с синдромом спинальной спастической параплегии инактивация триггерных точек способствует повышению порога Н-рефлекса, торможению спинального полисинаптического рефлекса и подавлению активности преимущественно низко- и высокопороговых мотонейронов. Чувствительность исследованных моно- и полиснаптических рефлексов к деструкции триггерных точек выше при гамма-ригидности или полной утрате супраспинального контроля.
Ключевые слова: триггерные точки, спинной мозг, мотонейроны, спастическая параплегия, Н-рефлекс, полисинаптический рефлекс.
Summary. At partial or complete infringement supruspinal control, the trigger points meet in cases much more often g -shiftiness and not characteristic for a -shiftiness. They do not depend on a degree of a defeat of a back brain and presence of frustration of deep or superficial kinds of sensitivity.
At the patients with syndrome of spinal spastically lower paralysis the destruction of trigger points promotes increase of a threshold of a Н-reflex, braking spinal multisinaptical reflex and suppression of activity mainly low and high thresholdli motoneurons. The sensitivity investigated mono- and multisinaptical reflex to destruction of trigger points is higher at g -stifnistis or complete loss supruspinal control.
Keywords: trigger points, back brain, motoneurons, spinal spastically paralysis, Н-reflex, multisinaptical reflex.
Введение, обзор литературы
В современной литературе под миофасциальной триггерной точкой (ТТ) подразумевают болезненную и гиперраздражимую при пальпации область нередко расположенную в уплотненном тяже скелетной мышцы или фасции - миофасциальном гипертонусе [19, 5].
Дж. Г. Тревелл и Д.Г. Симонс [19] утверждают, что в норме мышца не содержит ТТ и в них нет уплотненных тяжей.
При полном нарушении проводимости по периферическому нерву ТТ в зоне его автономной иннервации отсутствуют, однако. на определенном этапе регенерации нерва их количество в реиннервируемых тканях многократно возрастает [12, 13].
H. Bayer [22] и Л.З. Лауцевичус [8] считали, что в основе миофасциального гипертонуса лежит спинальный проприцептивный мышечный рефлекс. Г.А. Иваничев [5, 7] пришел к выводу, что диссоциированное расстройство поверхностных видов чувствительности за счет избирательного поражения боковых столбов спинного мозга (СМ) у больных сирингомиелией не нарушает процесса формирования болевых мышечных уплотнений. Этот факт послужил основанием для предположения о том, что дуга афферентных импульсов из ТТ проходит транзитно через СМ по путям глубокой чувствительности, замыкаясь в ростральных отделах ствола головного мозга, и, стало быть, при поражении задних столбов СМ миофасциальные гипертонусы не должны формироваться [5]. Последующие нейрофизиологические исследования [6, 7] подтвердили, что у больных с мышечными гипертонусами ирритативные процессы в стволе мозга преобладают над тормозными.
На заинтересованность диэнцефально-стволовых структур у больных с ТТ по данным электроэнцефалографических исследований указывает и В.Н. Шевага [21].
V. Janda [23] связывает отсутствие болезненности спазмированных мышц при патологии опорно-двигательного аппарата с дисфункцией лимбической системы.
В случаях экстрапирамидных гиперкинезов и дрожжательной формы паркинсонизма (патология подкорковых узлов) [15, 11, 12], а также при атактико-астатической форме детского церебрального паралича (поражение мозжечка с его связями или лобных долей) ТТ выявляются или в небольшом количестве, или вовсе отсутствуют [2]. При других формах церебрального паралича, характеризующихся главным образом задержкой формирования пирамидной системы и - как следствие - расторможенностью тоногенных стволовых центров, они локализуются в наиболее гипертоничных мышцах [2, 3].
Представленный обзор позволяет утверждать, что процесс формирования ТТ и сопутствующих им миофасциальных гипертонусов находится в явной зависимости от иерархического устройства центральной нервной системы (ЦНС) и тесно связан с ее спинально-стволовым уровнем.
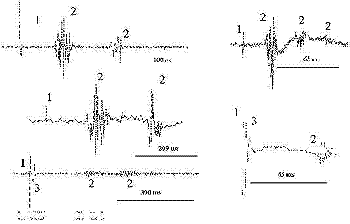
Рис. 1. Образцы записей полисинаптических рефлексов у больных с синдромом спинальной спастической парапрлегии. 1. раздражающий стимул. 2. Варианты полисинаптических ответов. 3. Случаи вызывания моносинаптических Н-рефлексов одновременно с полисинаптическим ответом
Материал и методы исследования
Особенности формирования ТТ в условиях изолированного СМ, а также их способность влиять на мышечный тонус и инициировать рефлексы спинального автоматизма была детально изучена нами на клинической модели - лицах с повреждением СМ на уровне шейного или грудного отделов позвоночника. Всего было обследовано 45 инвалидов-спинальников без значительных соматических осложнений (контрактуры, пролежни, пиелонефрит, выраженные нарушения дыхания и т.д.). В 23 случаях (51.1 %) диагностировалось полное нарушение проводимости по СМ, а в 22 (48.9 %) - частичное. Степень расстройства произвольных движений соответствовала абсолютной параплегии или глубокому парапарезу. Навык самостоятельной ходьбы отсутствовал во всех случаях. У всех больных диагностировались расстройства глубоких и поверхностных видов чувствительности различной степени выраженности.
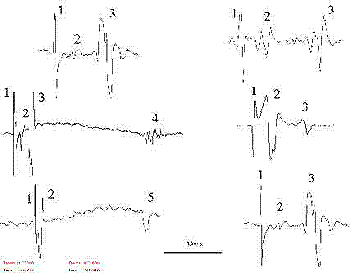
Рис. 2. Образцы записей Н-рефлексов у больных с синдромом спинальной спастиической параплегии.1. раздражающий ститмул. 2. М-ответ. 3. Моносинаптический Н-рефлекс. 4. Коротколатентный полисинаптический ответ. 5. Случай коротколатентного полисинаптического ответа вместо Н-рефлекса.
Признаки преимущественно гамма-ригидности (спастичности) выявлялись у 34 (75.56 %) обследованных, а преимущественно альфа-ригидности [16, 4, 17, 18, 10] - у 11 (24.44 %) человек.
В общей сложности у этих больных было изучено 1594 триггерных точки, в 93.3 % они обнаруживались в мышцах и фасциях. В большинстве случаев по кинестетическим признакам эти ТТ ничем не отличались от своих собратьев, выявляемых у лиц с сохранной ЦНС. Однако при наличии полной анестезии ниже уровня поражения СМ они нередко были лишены окружающего их миофасциального гипертонуса и определялись как индифферентные точечные участки, механическая стимуляция которых вызывает резкое повышение мышечного тонуса или активацию рефлексов спинального автоматизма.
На частоту встречаемости ТТ никак не влияли уровень и степень поражения СМ, а также характер чувствительных расстройств. Тем не менее, при альфа-ригидности ТТ выявлялись в значительно меньшем количестве, а нередко и вовсе отсутствовали. При стимуляции ТТ надавливанием в подавляющем большинстве наблюдений (97.51 %) инициировался сгибательный защитно-укоротительный рефлекс. При раздражении дистально расположенных точек (стопа, голень) интенсивность непроизвольных двигательных реакций была более значительной.
У 16 больных методами стимуляционной электромиографии проводилось исходное тестирование моно- и полисинаптических рефлексов СМ (в отличие от лиц с интактной нервной системой при спинальном спастическом синдроме полисинаптические ответы легко вызывается и регистрируется). Исследования повторялись сразу же после однократного сеанса инактивации ТТ на исследуемой нижней конечности, а также после окончания курса данных процедур. При этом для исключения следового действия локального анестетика была специально разработана методика лечебной пневмодеструкции триггерных точек [14].
С целью снижения потока висцерогенной афферентации, перед началом эксперимента больного просили опорожнить мочевой пузырь, а при необходимости ему накануне делалась очистительная клизма.
Моносинаптический Н-рефлекс исследовался по стандартной методике [1, 9]; анализировались следующие его характеристики: порог, латентный период, динамика изменения амплитуды при изменении силы стимуляции (кривая рекрутирования Н-рефлекса), процентное соотношение максимальных амплитуд Н-рефлекса и М-ответа (Нmax/Mmax*100%).
Спинальный полисинаптический рефлекс (СПР) исследовался у тех же больных, но на другой нижней конечности. В положении испытуемого на спине выявлялась ТТ с которой наиболее ярко вызывался спинальный защитно-укоротительный рефлекс. Над ней располагался биполярный раздражающий электрод. Регистрирующий электрод, соблюдая стандартные условия отведения, накладывался на переднюю большеберцовую мышцу исследуемой конечности. Раздражение производилось одиночными импульсами длительностью 0.5 - 1.0 мс. Анализировались порог, латентность, длительность и максимальная амплитуда полисинаптического рефлекса. Максимальная эпоха анализа потенциалов соответствовала 2.4 сек (8640 мс). Аналогичному тестированию подвергались акупунктурные точки и просто индифферентные участки кожной поверхности.
Учитывая вариабельность рассматриваемых показателей, среднее значение каждого параметра в обоих методиках вычислялись не менее чем по результатам 10 измерений у каждого больного (Рис. 1, 2). При статистической обработке материала применялось сравнение выборок по парному критерию Вилкоксона и корреляционный анализ [20].
Результаты исследования параметров Н-рефлекса
В исходном состоянии данный рефлекторный феномен у больных с синдромом спинальной спастической параплегии характеризовался порогом вызывания в 179.69 + 24.23 V, латентностью в 31.66 + 1.11 мc и отношением Нmax/Mmax*100%, равным 49.83 %. После однократной пневмодеструкции ТТ статистических различий между параметрами Н-рефлекса выявлено не было. После окончания всего курса лечения отмечалось уменьшение возбудимости мотонейронов в среднем на 3.85 % относительно исходных значений (P < 0.05), а также снижение порога вызывания Н-рефлекса на 9.3 V (P < 0.1).
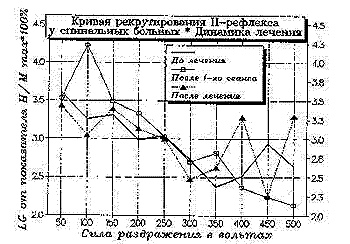
Рис. 3. Кривые рекрутирования Н-рефлекса у больных с синдромом спинальной спастической параплегии. Динамика лечения методом пневмодеструкции триггерных точек.
Кривые рекрутирования Н-рефлекса при спинальном спастическом синдроме имели общую тенденцию к обратно пропорциональной зависимости от напряжения раздражающего тока (Рис. 3), что свидетельствует о преобладании доли потенциально возбудимых низкопороговых мотонейронов над высокопороговыми в исследуемом мотонейронном пуле. На этом фоне в исходном состоянии наблюдается повышение активности части высокопороговых мотонейронов с уровнем возбудимости в 450 V, кроме того методом линейной корреляции выявлены тесные положительные функциональные взаимосвязи между средне- и высокопороговыми мотонейронами, активирующимися при раздражении в 250 - 500 V (среднее R = 0.73).
После однократного сеанса пневмодеструкции наблюдалось незначительное, но достоверное снижение числа возбудимых низкопороговых мотонейронов (для порога в 50 V - на 0.4 % при P < 0.05). Положительные корреляционные связи были найдены между среднепороговыми мотонейронами, возбуждающимися при 150 - 350 V (среднее R = 0.72).
После окончания курса лечебной пневмодеструкции, по сравнению с исходным состоянием, наблюдалось снижение процента возбудимых как низко-, так и высокопороговых мотонейронов: для порога в 50 V - на 10.14 % и для порога в 450 V - на 9.14 % (при Р < 0.1); а также некоторое возрастание активности среднепороговых мотонейронов: для порога в 200 V - на 4.8 % (при Р < 0.1). В сравнении с состоянием “после однократного сеанса пневмодеструкции” наблюдалось статистически достоверное уменьшение числа возбудимых среднепороговых мотонейронов: для порога в 200 V - на 12.13 % (при P <=0.03), для порога в 250 V - на 2.8 % (при P <= 0.09) и для порога в 350 V - на 5.12 % (при P <= 0.13). Отмечены корреляционные связи преимущественно в спектре высокопороговых мотонейронов - 300-450 V (среднее R = 0.73).
Результаты исследования параметров спинального полисинаптического рефлекса
В рамках этого эксперимента было проанализировано более 2500 записей СПР. Изучаемый рефлекс в данном контингенте больных имел порог вызывания в 364.25 + 11.81 V, представляя собой вспышку биоэлектрической активности с латентным периодом в 316.27 + 39.23 мc, длительностью 270.69 + 18.44 мc и максимальной амплитудой 55.58 + 5.31 mV (Рис. 1). Каких-либо статистических различий в параметрах полисинаптического ответа при электрическом раздражении ТТ, акупунктурных точек и индифферентных мягких тканей выявлено не было.
После однократного сеанса пневмодеструкции отмечено достоверное уменьшение длительности СПР на 13.9 % по сравнению с исходным состоянием (P <= 0.03), а после окончания всего курса лечения – на 45.81 % (при P <= 0.0008). Латентный период после лечения удлинился в 2.6 раза по сравнению с исходным состоянием (при P <= 0.04). Максимальная амплитуда рефлекса снизилась после лечения на 45.1 % (Р <= 0.005), ее уменьшение по сравнению с однократным сеансом составило 48.8 % (Р <= 0.005).
При сравнении больных с полным и частичным нарушением проводимости по СМ установлено, что исходная латентность СПР в первом случае на 25.8 % (Р <= 0.08) выше чем во втором. В результате лечения эти различия еще более усугублялись, составляя как после однократного сеанса, так и после курса пневмодеструкции около 39 % (Р < 0.02). Итоговый прирост данного показателя в обеих группах был равен соответственно 193.5 % и 141.6 %.
После однократного сеанса пневмодеструкции отмечено возрастание максимальной амплитуды СПР при частичном нарушении проводимости по СМ на 20.6 % относительно исходного состояния, что превышало аналогичные показатели для полного нарушения в 1.5 раза (Р <= 0.05). В результате проведенного курса лечения выяснилось, что порог вызывания СПР при полном поражении СМ стал выше на 14.1 %, относительно частичного поражения (Р <= 0.06).
При сравнении больных с преимущественными проявлениями гамма- и альфа-ригидности исходный порог вызывания СПР был выше на 15.9 % (Р <= 0.02), а его длительность - ниже на 33.9 % (Р <= 0.01) в первом случае. После однократного сеанса пневмодеструкции длительность СПР уменьшилась в обеих группах, сохраняя более низкие показатели при гамма-ригидности (Р <= 0.1). По окончании курса лечебной пневмодеструкции статистически достоверных различий в параметрах СПР между сравниваемыми вариантами патологического повышения мышечного тонуса выявлено не было.
Обсуждение полученных результатов
Таким образом, полученные результаты свидетельствуют, что при частичном или полном нарушении супраспинального контроля ТТ гораздо чаще встречаются в случаях гамма- и не характерны для альфа-ригидности. Они не зависят от степени поражения спинного мозга и наличия расстройств глубоких или поверхностных видов чувствительности.
В процессе пневмодеструкции ТТ имеется тенденция к снижению порога Н-рефлекса и уменьшению процента возбуждающихся мотонейронов. Инактивация ТТ способствует подавлению активности преимущественно низко- и высокопороговых мотонейронов. Наиболее тесные функциональные связи при вызывании Н-рефлекса выявлены между средне- и высокопороговыми мотонейронами.
При вызывании СПР, стимуляция ТТ электрическим током не имеет никаких преимуществ над аналогичным раздражением индифферентных участков кожи. Этот факт подтверждает версию о том, что электрический импульс, в отличии от механического, не является специфическим раздражителем ТТ.
В процессе инактивации ТТ наблюдаются признаки подавления СПР: повышение порога, увеличение латентного периода, уменьшение длительности и амплитуды. Уровень активности СПР ниже, а его чувствительность к деструкции ТТ выше в случаях гамма-ригидности или полной утраты супраспинального контроля.
Способность ТТ укорачивать латентные периоды на 20 - 30 % по сравнению с нормой подтверждается и Г.А. Иваничевым [6, 7], изучавшим спинально-стволовой полисинаптический рефлекс у больных остеохондрозом позвоночника. По его мнению данный факт является следствием включения релейных структур каудальной ретикулярной формации ствола, благодаря чему импульс преодолевает более короткий путь. В наших случаях число синаптических переключений было ограничено уровнем поражения СМ, поэтому мы склонны связывать это явление с облегчением проводимости по толстым скоростным низкопороговым афферентным волокнам.
Представленные результаты свидетельствуют, что в отличие от обычных экстерорецепторов ТТ обладают более избирательной реактивностью к механической стимуляции, а также подтверждают их роль в сегментарных и проприоспинальных двигательных рефлексах.
По-видимому, минимальным дискретом, необходимым для реализации ТТ и окружающего его миофасциального гипертонуса, является сегмент СМ, кроме того они могут успешно проявляться с помощью проприоспинальных и стволовых связей, однако никак не влияют на деятельность вышележащих отделов ЦНС, в частности - подкорковых образований и коры.
Список литературы
1. Бадалян Л.О., Скворцов И.А. Клиническая электромиография.- М., Медицина, 1986.- 368 с.
2 . Богданов Э.И., Мухамедзянов Р.З. Миофасциальные гипертонусы у больных с последствиями перенатальных поражений центральной нервной системы в позднем резедуальном периоде.// Третий международный конгресс вертеброневрологов.- Казань, 1993.- С.12-13.
3. Бортфельд С.А. Двигательные нарушения и лечебная физкультура при детском церебральном параличе. - Л., Медицина, 1971. - 247 с.
4. Гранит Р. Основы регуляции движений / пер. с англ. - М., Мир, 1973. - 368 с.
5. Иваничев Г.А., Хасанова Р.Б., Алеева Л.Л. Роль мышечного фактора в патогенезе альгических форм сирингомиелии.// Ж. Невропатол. и психиатр.- 1982.- No 4.- С.529-532.
6. Иваничев Г.А. Болезненные мышечные уплотнения. - Казань, 1990. - 157 с.
7. Иваничев Г.А. Контрактура мимической мускулатуры. - Казань, 1992. - 108 с.
8. Лауцевичус Л.З. Исследование болевого синдрома при поражении скелетных мышц и применение нового метода сегментарно-рефлекторной терапии.// Успехи медицинской науки в Советской Литве.- Вильнюс, 1971. - С.56 - 95.
9. Манович З.Х. О некоторых методических положениях применения стимуляционной электромиографии в клинике.// Параклинические методы исследования в неврологической клинике. вып. 1.: Клиническая электроэнцефалограяия и электромиография/ под ред. Е.А. Журманской (Всесоюзный симпозиум - ноябрь 1969).- М., 1969. - С. 169 - 177.
10. Несмеянова Т.Н. Стимуляция восстановительный процессов при травме спинного мозга.- М.,Наука, 1971.- 255 с.
11. Петров Б.Г. Особенности клиники поясничного сотеохондроза у больных паркинсонизмом и патогенез мышечной контрактуры.// Синдромы позвоночного остеохондроза.- Казань, 1978.- С.90 - 92.
12. Петров К.Б. Физиология триггерных точек и патогенез триггерных болей: Сообщение первое.// Мануальная медицина. – Nо 9. - Новокузнецк, 1995. - С.9 - 14.
13. Петров К.Б. К семиотике и прогностике компрессионных корешковых синдромов у больных поясничным остеохондрозом. // Тезисы Всероссийской юбилейной научно-практической конференции, посвященной 70-ти летнему юбилею городской клинической больницы No 1 г. Новокузнецка (25 ноября 1999 г.) - Новокузнецк, 1999. - С. 130- 131.
14. Петров К.Б. Способ лечения миофасциальных болевых синдромов методом пневмодеструкции триггерных точек.// Медицина на ружеже веков: Сборник трудов, посвященный 70-летнему юбиолею Многопрофильной клинической больницы Nо 2 г. Новокузнецка.- Новокузнецк, - 1999.- С.207 - 210.
15. Попелянский Я.Ю. Паркинсонизм и шейный остеохондроз.// Остеохондрозы позвоночника. Выпуск 2: Материалы Второго Новокузнецкого симпозиума по дегенеративным заболеваниям межпозвонковых дисков (26 - 29 октября 1966 г.).- Новокузнецк, 1966. - С.107-118.
16. Росси Дж.Ф., Цанкетти А. Ретикулярная формация ствола мозга /пер. с англ.- М., издательство иностранной литературы, 1960.- 263 с.
17. Семенова К.А. Детские церебральные параличи.- М., Медицина, 1968.- 259 с.
18. Старобинец М.Х., Волкова Л.Д. Методические приемы определения альфа- и гамма- форм спастичности при пирамидном синдроме.// Современные методы исследования в неврологии и психиатрии.
Т. 2.: Тезисы докладов научно-практической конференции (май 1977 г.).- Курск, 1977.- С. 151 - 152.
19. Тревелл Дж.Г., Симонс Д.Г. Миофасциальные боли. Т. 1. / Пер. с англ.- М., Медицина, 1989. - 240 с.
20. Тюрин Ю.Н., Макаров А.А. Анализ данных на компьютере/ под ред. В.Э. Фигурнова.- М., ИНФРА-М, Финансы и статистика, 1995.- 348 с.
21. Шевага В.Н. К вопросу о патогенезе миофасциальной боли.// Мануальная медицина.- No. 6.- Новокузнецк., 1994. - С. 6.
22. Bayer H. Die rheumatische Muskelharte - Eigenreflextetanus.// Klin. Wochenschr. - 1949.- No. 27.- P. 122 - 126.
23. Janda V. Mascle spasm - a proposed procedure for differential diagnosis.// J. Manual medicine. - 1991.- No. 6.- C. 136-139.
Опубликовано: Петров К.Б. Сегментарные и проприоспинальные механизмы патогенеза миофасциальных триггерных точек // Вертеброневрология. - Том 8.- №. 1 - 2. - Казань, 2001. - С. 19 - 25.






