Современная тактика лечения больных злокачественными новообразованиями с метастазами в кости. Часть 1
НИИ онкологии им. проф. Н.Н. Петрова
Пособие для врачей посвящено современному паллиативному лечению больных с метастатическим поражением костей при солидных опухолях.
Использование препаратов группы бисфосфонатов, оказывающих лечебное действие при болевом синдроме, гиперкальциемии, а также позволяющих предупреждать их появление, патологических деформаций, переломов, открывает перспективу улучшения качества жизни этой категории больных.
Пособие предназначено для онкологов, терапевтов и студентов медицинских институтов.
ФОРМУЛА МЕТОДА
Новизна предлагаемой авторами методики заключается в использовании лекарственного препарата (Клодронат) с принципиально новым механизмом действия в режиме (однократная 4-часовая инфузия) оптимальном с медицинской и организационной точек зрения для больных с множественными метастазами в кости.
ВВЕДЕНИЕ
Злокачественные опухоли нередко сопровождаются поражением костей и нарушениями минерального обмена (в том числе кальциевого гомеостаза). Боли в костях, патологические переломы и гиперкальциемия являются важнейшими клиническими проявлениями этого процесса, они в значительной степени отвественны за тяжесть состояния больных и в ряде случаев являются причиной смерти. Эти клинические симптомы часто наблюдаются при наличии остеолитических метастазов, но могут быть и при ге-нерализованном остеолизе, развивающемся вследствие эктопической продукции гормонов некоторыми солидными опухолями.
Независимо от того имеет ли место местный или гене-рализованный остеолиз, патогенез усиленной костной резорбции обусловлен нарушениями нормального механизма костеобразования. В основе его лежит активизация резорбтивных процессов в костной ткани вследствие “регулирующего” влияния метастатических клеток.
Этот недавно установленный факт послужил основанием для изучения возможностей использования с лечебной целью в клинической онкологии лекарственных препаратов, которые обладают способностью оказывать влияние не столько на метаболизм самой опухоли, сколько на костный обмен, нарушенный опухолевым процессом. Несмотря на то, что предлагаемое лечение не является собственно цитотоксическим и не направлено непосредственно против раковых клеток, это один из реальных путей повышения качества жизни пациентов.
Подобным механизмом действия обладают митрами-цин, нитрат галлия, ингибиторы синтеза простагландинов (аспирин,индометацин), кальцитонин и бисфосфонаты. Бисфосфонаты представляются наиболее перспективными в связи со способностью ингибировать на длительное время костную резорбцию.
ОПИСАНИЕ МЕТОДА
МЕХАНИЗМ ОБРАЗОВАНИЯ И РЕЗОРБЦИИ КОСТНОЙ ТКАНИ
Костная ткань характеризуется динамичностью и постоянной перестройкой, имеет высокую васкуляризацию (до 10% сердечного выброса проходит через неё) и не является “мертвой”, как это было принято считать раньше.
Структура кости представлена органическим матриксом (35%), минеральной частью (65%) и клетками. Органический матрикс на 90-95% состоит из коллагена типа I, на 5-10% из протеинов сыворотки (альбумины и др.) и ряда других белков (остеокальцин.остеонектин и др.). Минеральная часть матрикса содержит гидроксиапатит [Са^(ОН)^(Р04)б], в котором отмечается большое количество кальция и фосфора.
Кость формируется клетками мезенхимального происхождения - остебластами, синтезирующими и секретиру-ющими органический матрикс. Минерализация матрикса продолжается несколько недель.
Резорбция кости осуществляется остеокластами которые являются многоядерными клетками, формирующимися изначально из гематопоэтических стволовых клеток. Процесс резорбции происходит в “гребешковых” пространствах, где остеокласты прикрепляются к костному мат-
риксу и формируют специальную фестончатую линию. Минеральные составляющие и органический матрикс элиминируются именно в этом месте. В области фестончатой линии обнаружены протеины, ответственные за создание особой кислой среды в прилежащем экстрацеллюлярном пространстве, которая обеспечивает растворение минеральной части костной ткани.
Органическая часть костного матрикса резорбцирует-ся с помощью кислых гидролаз вслед за растворением минеральной части.
Перестройка (разрушение и образование) костной ткани является циклическим процессом, постоянно и одновременно происходящим в тысячах мест скелета и, в среднем, полное обновление его у человека отмечается каждые 10 лет. У взрослых в связи с прекращением роста костей в длину около 95% костного обмена связано именно с перестройкой этого органа, которой в любое время подвергается приблизительно 10-15% всей костной поверхности .
Процесс перестройки предполагает определенную последовательность циклических событий, при которых фаза костной резорбции обязательно предшествует фазе кос-теобразования.
Эта последовательность (рисунок 1) наблюдается на поверхности как кортикальной (компактной), так и трабе-кулярной кости. Фаза активизации остеокластов с последующей резорбцией кости завершается образованием эрозивной полости. Появление в ней мононуклеарных клеток означает переход к следующей фазе цикла перест-
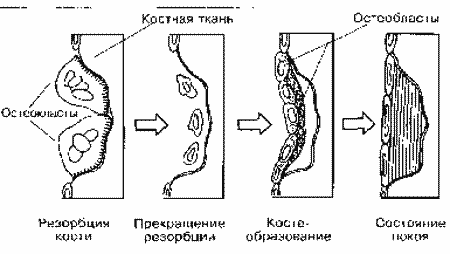
Рис. 1. Процесс перестройки костной ткани
ройки. Эти клетки обладают способностью перемещаться из эрозивной полости и, вероятно, передавать сигнал, который привлекает остеобласты в зону резорбции. Остеобласты направляются к этой области и начинают синтезировать остеоидный матрикс, который затем минера-лизуется.
В среднем во взрослом человеческом организме содержится около 1-2 кг кальция, 98% которого находится в скелете в виде нерастворимого гидроксиапатита.
Содержание кальция в межтканевой жидкости является важной константой, так как имеет критическое значение для ряда функций.
В норме у взрослых уровень кальция в плазме колеблется от 2,2 до 2,6 mmol/L.
МЕТА СТАТИЧЕСКОЕ ПОРАЖЕНИЕ КОСТЕЙ
Таблица 1.Частота метастатического поражения костей по данным аутопсий пои опухолях оазличных локализаций
| Локализация опухоли | Частота метастазов в кости(в %) |
| Молочная железа | 47-85 |
| Предстательная железа | 54-85 |
| Щитовидная железа | 28-60 |
| Почка | 33-40 |
| Легкие | 32-40 |
| Печень | 16 |
| Яичники | 9 |
| Пищевод | 5-7 |
| Прямая кишка | 8-13 |
| Шейка матки | 0 |
Костная ткань является объектом метастазирования, как и все другие ткани. Наиболее часто в кости метастазиру-ют рак молочной и предстательной железы, легкого, щитовидной железы и почки (таб. 1). При этом метастазами преимущественно поражаются позвоночник, проксималь-ная часть бедренной и плечевой костей, кости таза, ребра, грудина.
Как видно из таблицы 2, метастазы распространяются преимущественно по оси скелета, что, в основном, отражает особенности распределения красного костного мозга. Однако, только присутствия опухолевых клеток в сосудах костного мозга недостаточно для развития собственно метастатического очага, необходимы еще определенные биологические условия. Одним из важнейших условий является повышенная экспрессия паратгормонподобного белка, который может выделяться опухолевыми клетками и как паратгормон способен активизировать костный обмен.
Таблица 2. Особенности метастатического поражения скелета при раке молочной железы
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
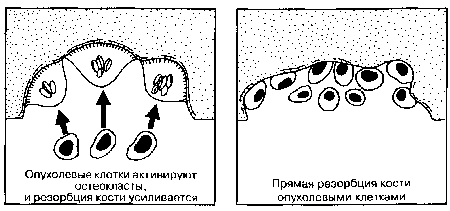
Рис. 2. Два механизма остеолиза при солидных опухолях
Костные метастазы могут быть остеолитическими, осеобластическими и смешанными.При наличии остеолитических поражений разрушение кости (остеолиз) происходит ( рисунок 2) :
• вследствие повышенной активности остеокластов, стимулируемых опухолевыми клетками, которые выделяют простагландины, прокатепсин D, трансформирующие факторы роста;
• путем прямого разрушения костной ткани раковыми клетками с помощью секреции коллагеназы и других ферментов.
При раке молочной железы костная резорбция, в основном, обусловлена первым механизмом и сопровождается увеличением числа и повышением активности остеокластов,то есть разрушение кости происходит собственными нормальными клетками. Прямой остеолиз имеет место редко, преимущественно на поздних стадиях.
При развитии остеобластических метастазов новая костная ткань образуется остеобластами, также активированными веществами, выделяемыми опухолевыми клетками. Причем, в результате этого процесса костеобра-
зование носит “ненормальный” характер, и плотность образующейся костной ткани может быть выше обычной. Подобное увеличение плотности рентгенологически может симулировать остеосклероз.
Особенности метастатического поражения костей при различных опухолях представлены в таблице 3.
Остеолитические метастазы с деструкцией костного матрикса могут сопровождаться гиперкальциемией и ги-перкальциурией. При этом уровень в сыворотке щелочной фосфатазы бывает нормальным или слегка повышенным. Остеобластические метастазы вызывают выраженное повышение щелочной фосфатазы и могут сопровождаться гипокальциемией. Необходимо иметь ввиду, что при некоторых костных метастазах (например, рака молочной железы) может быть фаза, при которой преобладает остеолиз (с гиперкальциурией, гиперкальциемией и нормальным уровнем щелочной фосфатазы), за которой следует фаза с высоким уровнем щелочной фосфата-зы и появлением склеротических очагов.
Таблица 3. Особенности метастатического поражения костей при различных онкологических заболеваниях
| Характер опухоли | Остеолитические метастазы | Остеобластические метастазы |
| Рак молочной железы | + | + |
| Рак предстательной железы | - | + |
| Лимфогранулематоз (болезнь Ходжкина) | - | + |
| Неходжкинские лимфомы | + | - |
Клиническая картина метастазов в кости при злокачественных опухолях включает в себя болевой синдром, деформации и патологические переломы, а также гипер-кальциемию. Исключительно редко метастатическое поражение костей бывает бессимптомным.
Боль является одним из наиболее значимых признаков метастатического поражения костей. Болевой синдром имеет место в течение жизни у 70% больных с метастаза-ми в кости. Адекватное обезболивание при этом крайне затруднительно без использования наркотических аналь-гетиков. Проведение лучевой терапии в ряде случаев бывает эффективным, однако, возможности его ограничены в связи с частой необходимостью повторного облучения, значительной диссеминацией очагов поражения, а также мигрирующим характером болей. Между тем, труднопе-реносимые боли требуют назначения высоких доз наркотических анальгетиков и часто госпитализации.
Патогенез болевого синдрома у больных с метастаза-ми в кости остается недостаточно понятным. Следует учитывать, что кортикальный слой и костный мозг не имеют чувствительных рецепторов, поэтому болевая импульса-ция может исходить только из надкостницы.
Предполагается несколько возможных механизмов развития болевого синдрома:
• во-первых, боль может быть следствием опухолевой инфильтрации нервных окончаний:
• во-вторых, механической стимуляции рецепторов из-за растяжения тканей вследствие повышения внутри-костного давления растущим метастазом, субклинического или клинического перелома и т.д.;
• в-третьих, имеет значение химическая стимуляция рецепторов биологически активными пептидами, в первую очередь, простагландинами (PGE, и PGE^), высвобождаемыми в больших количествах при остеолизе. Последний механизм является доминирующим. Кроме того, у некоторых больных болевой синдром может быть одновременно обусловлен несколькими механизмами. Например,вследствие увеличения внутрикостного давления из-за роста метастатического узла и стимуляции сот-ветствующих рецепторов может произойти выброс медиаторов, в том числе, простагландинов.
Гиперкальциемия является вторым важнейшим симп-томокомплексом метастазов в кости, характерным, однако, преимущественно для остеолитического варианта.
Гиперкальциемия, по данным литературы, наблюдается у 10-15% больных злокачественными опухолями. Несколько чаще она бывает при раке молочной железы (30-40%), раке легкого ( 20% ). Причем три вида опухолей (рак молочной железы, легкого и мочевого пузыря) ответственны более чем за половину всех случаев гиперкальциемии, регистрируемых у больных с солидными неоплазмами.
Истинная частота этого состояния может быть значительно выше в связи с тем, что электролитный мониторинг у больных с множественными костными метастазами
на практике проводится редко. А характерный для гипер-кальциемии симптомокомплекс у терминальных больных часто расценивается как “прогрессирование основного заболевания”.
Клиническая картина гиперкальциемии включает общую и мышечную слабость, депрессию, психические нарушения, атаксию, анорексию, тошноту, рвоту, запоры, гипотонию, полиурию, изменения на ЭКГ (укорочение интервала QT) и у некоторых больных - аритмии. Гиперкальци-емия и гиперкальциурия оказывают негативное влияние на почечную функцию и приводят, в первую очередь, к нарушению способности концентрировать мочу (полиу-рия). Вследствие этого уменьшается объем внеклеточной жидкости (дегидратация), что в свою очередь усугубляет нарушенную клубочковую фильтрацию, что завершается развитием выраженных морфологических изменений. Если не производится коррекция гиперкальциемии последовательно развиваются дегидратация, почечная недостаточность, кома и смерть. В случае адекватного лечения этого осложнения и последующей профилактики рецидивов больные могут жить в течение многих месяцев и даже лет.
Наличие или отсутствие клинических симптомов, а также их выраженность мало зависит от степени гиперкальциемии.
В основном клинические симптомы появляются при уровне кальция в сыворотке выше 2.9—3.0 mmol/L, но некоторые больные даже при таком уровне кальция не отмечают каких-либо жалоб.
Гиперкальциемию 3.7 mmol/L или выше принято считать тяжелой. Такое состояние требует неотложного лечения.
Когда уровень кальция становится равным 3.7—4.5 mmol/L или выше, развивается кома и остановка сердца.
Известно два механизма развития гиперкальциемии у больных солидными опухолями. Гиперкальциемия может быть вследствие:
• локальной метастатической деструкции кости;
• генерализованного остеолиза, обусловленного выделением опухолью некоторых гуморальных факторов.
В обоих случаях наблюдается усиление костной резорбции. Отличительной чертой второго является повышенная почечная реабсорбция кальция, которая играет доминирующую патогенетическую роль .
Гуморальная гиперкальциемия наблюдается чаще у больных раком легкого и почки, у которых могут отсутствовать метастазы в кости. В этом случае клиническая картина соответствует гиперпаратиреоидизму и удаление или регрессия первичной опухоли под влиянием цитоста-тической терапии приводит к исчезновению этого состояния. Главной причиной его является секреция опухолевой тканью паратгормонподобного белка.
Рак молочной железы является типичной солидной опухолью, которая вызывает гиперкальциемию вследствие локальной остеолитической деструкции, обусловленной местной стимуляцией остеокластов продуктами, секрети-руемыми метастатическими раковыми клетками. Предположительно, что такими веществами, как и в случае болевого синдрома, могут быть простагландины Е, которые являются одними из основных потенциальных стимуляторов остеокластов.
Деформации и патологические переломы наряду с болевым синдромом и гиперкальциемией являются характерными для клинической картины метастазов в кости.
Приблизительно у 25% больных раком молочной железы с метастазами в кости наблюдаются патологические переломы длинных трубчатых костей. Присутствие в костях метастазов сопровождается выраженными функциональными и косметическими нарушениями и в конечном счете являются главной причиной значительного ухудшения качества жизни онкологических больных, более того, может стать причиной смерти. Наиболее частым является перелом позвонков, который сопровождается усилением болей, кифозом, снижением роста и параплегией.
При тщательном поиске переломы позвонков могут быть выявлены у 46% больных метастатическим раком молочной железы.
Другой частой локализацией патологических переломов являются ребра и проксимальные части плечевой и бедренной костей. Однако они наблюдаются в 3 раза реже, чем переломы позвонков. Риск патологических переломов в длинных трубчатых костях коррелирует со степенью деструкции кортикального слоя. Перелом становится вероятным при разрушении кортикального слоя более,чем на 50%.
Больные солидными опухолями с метастазами в кости имеют плохой прогноз. Например, при немелкоклеточном раке легкого медиана выживаемости не превышает 3 месяцев. Однако при некоторых гормоночувствительных опухолях (раке предстательной и молочной железы) показатели выживаемости при метастазах в кости значительно более высокие и являются благоприятным прогностическим признаком по сравнению с поражением висцеральных органов (медиана выживаемости при метастазах в кости составляет 24 месяца, а при метастазах в печень — лишь 3 месяца).
Относительно продолжительная выживаемость этих больных делает высокоактуальным проведение эффективного паллиативного лечения, имеющего целью улучшение качества жизни пациентов.
В практической деятельности при наличии метастазов в кости проводится стандартное противоопухолевое лечение (химиотерапия, гормонотерапия) в зависимости от локализации первичной опухоли. При наличии выраженного болевого синдрома дополнительно проводится симптоматическое лечение ненаркотическими и/или наркотическими анальгетиками. Часто с успехом используется также лучевая терапия. Однако этот метод имеет существенные ограничения, которые не позволяют считать его перспективным:
• во-первых, в связи с тем, что эффект лучевой терапии ограничивается только обезболиванием (возможность профилактики патологических переломов и гиперкаль-циемии отсутствует);
• во-вторых, в связи с трудностями достижения удовлетворительного анальгетического эффекта при наличии множественных метастазов (что, как правило, имеет место);
• в-третьих, в связи с частой необходимостью госпитализации этой категории больных из-за трудностей облучения в амбулаторных условиях. Всех перечисленных недостатков лишены бисфофона-ты. Препараты этой группы открывают несомненные перспективы в паллиативном лечении больных с метастаза-ми в костях.
>>часть 2 (в работе)